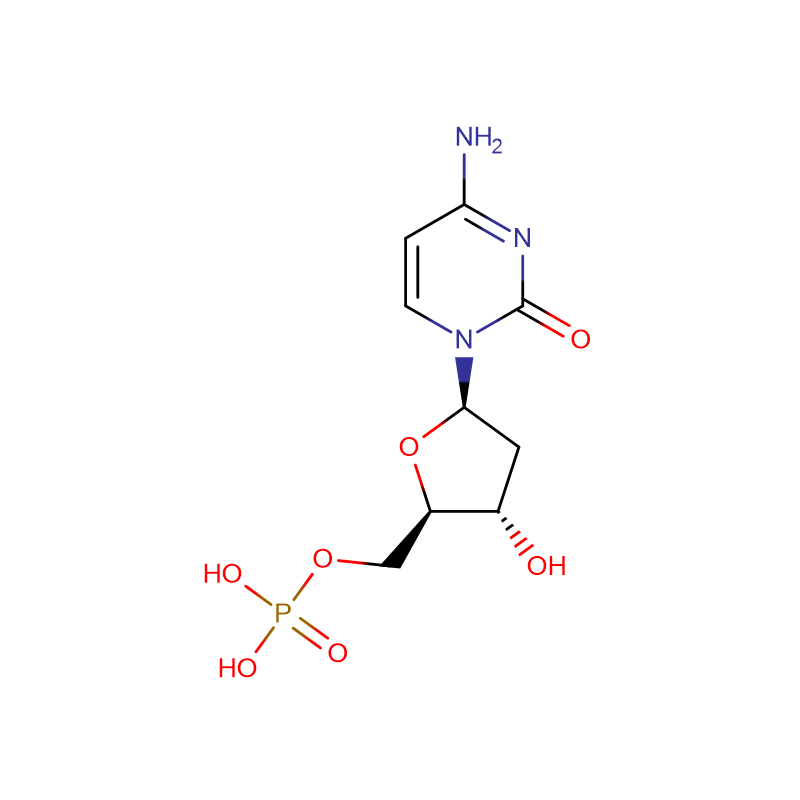
2'-deossiuridina Cas:951-78-0
| Numero di catalogo | XD90583 |
| nome del prodotto | 2'-deossiuridina |
| CAS | 951-78-0 |
| Formula molecolare | C9H12N2O5 |
| Peso molecolare | 228,20 |
| Dettagli di archiviazione | da 2 a 8 °C |
| Codice tariffario armonizzato | 29349990 |
Specifiche di prodotto
| Aspetto | Polvere da bianca a biancastra |
| Saggio | 99% |
| Punto di fusione | 164 - 168 gradi C |
| Perdita all'essiccamento | <1,0% |
| Residuo all'accensione | <0,1% |
Un migliore utilizzo dell'azoto nei bovini è importante per garantire una produzione bovina sostenibile.Poiché le purine e le pirimidine (PP) costituiscono una parte apprezzabile dell'azoto ruminale, è essenziale una migliore comprensione dell'assorbimento e del metabolismo intermedio del PP.Il presente lavoro descrive lo sviluppo e la convalida di un metodo sensibile e specifico per la determinazione simultanea di 20 purine (adenina, guanina, guanosina, inosina, 2'-deossiguanosina, 2'-deossiinosina, xantina, ipoxantina), pirimidine (citosina, timina, uracile, citidina, uridina, timidina, 2'-deossiuridina) e i loro prodotti di degradazione (acido urico, allantoina, β-alanina, acido β-ureidopropionico, acido β-amminoisobutirrico) nel plasma sanguigno delle vacche da latte.La tecnica basata sulla cromatografia liquida ad alte prestazioni accoppiata alla spettrometria di massa tandem a ionizzazione elettrospray (LC-MS/MS) è stata combinata con singoli standard di calibrazione abbinati a matrice e composti di riferimento etichettati isotopicamente stabili.L'analisi quantitativa è stata preceduta da una nuova procedura di pretrattamento costituita da precipitazione, filtrazione, evaporazione e ricostituzione dell'etanolo.Sono stati studiati i parametri per la separazione e il rilevamento durante l'analisi LC-MS/MS.È stato confermato che l'utilizzo di un modello di calibrazione logaritmica piuttosto che di un modello di calibrazione lineare ha comportato un CV% inferiore e una mancanza di test di adattamento ha dimostrato una regressione lineare soddisfacente.Il metodo copre gli intervalli di concentrazione per ciascun metabolita in base a quelli dei campioni effettivi, ad esempio guanina: 0,10-5,0 μmol/L e allantoina: 120-500 μmol/L.Il CV% per gli intervalli di quantificazione scelti era inferiore al 25%.Il metodo ha una buona ripetibilità (CV%≤25%) e precisione intermedia (CV%≤25%) e ottimi recuperi (91-107%).Tutti i metaboliti hanno dimostrato una buona stabilità a lungo termine e una buona stabilità all'interno delle analisi (CV%≤10%).Diversi gradi di effetti matrice assoluti sono stati osservati nel plasma, nelle urine e nel latte.La determinazione dei relativi effetti matrice ha rivelato che il metodo era adatto a quasi tutti i metaboliti PP esaminati nel plasma prelevato da un'arteria e dalle vene portali epatiche, epatiche e gastrospleniche e, con poche eccezioni, anche per altre specie come pollo, maiale, visone, umano e topo.