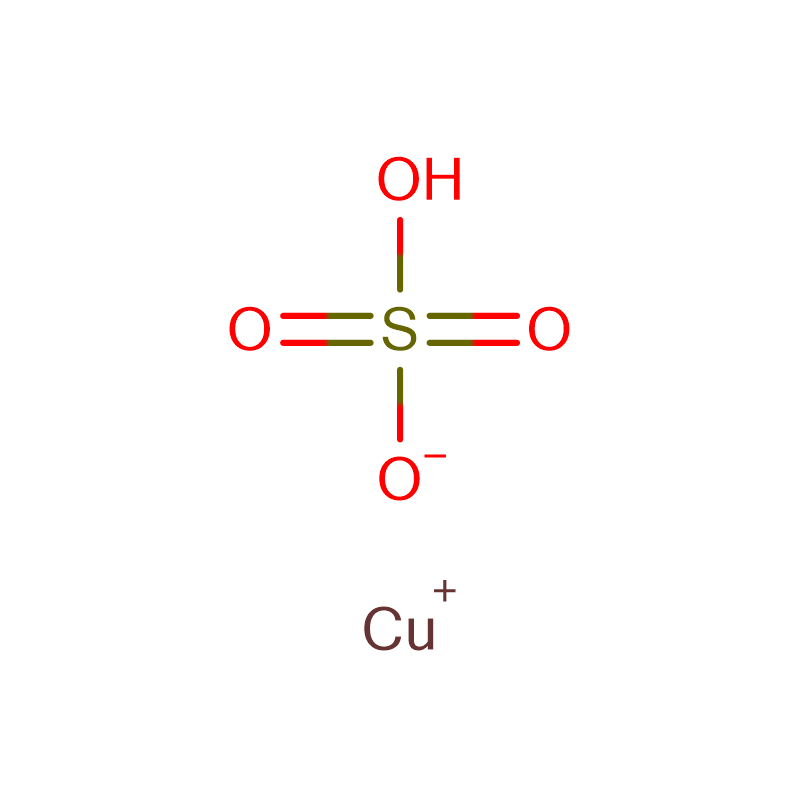
Solfato di rame pentaidrato Cas: 7758-98-7
| Numero di catalogo | XD91844 |
| nome del prodotto | Solfato di rame pentaidrato |
| CAS | 7758-98-7 |
| Formula Molecolarela | CuO4S |
| Peso molecolare | 159,61 |
| Dettagli di archiviazione | 5-30°C |
| Codice tariffario armonizzato | 28332500 |
Specifiche di prodotto
| Aspetto | Polvere da verdastra a grigia |
| Assy | 99% min |
| Mpunto di fuga | 200 °C (dec.)(lett.) |
| densità | 3,603 g/mL a 25 °C (lett.) |
| pressione del vapore | 7,3 mmHg (25 °C) |
| solubilità | H2O: solubile |
| Peso specifico | 3.603 |
| PH | 3.5-4.5 (50g/l, H2O, 20℃) |
| Gamma pH | 3.7 - 4.5 |
| Solubilità dell'acqua | 203 g/L (20ºC) |
| Sensibile | Igroscopico |
| Stabilità | igroscopico |
Utilizzato come antimicrobico e molluschicida.
Il solfato di rame è anche noto come vetriolo blu, questa sostanza è stata prodotta dall'azione dell'acido solforico sul rame elementare.I cristalli blu brillante sono solubili in acqua e alcool.Mescolato con ammoniaca, il solfato di rame veniva utilizzato nei filtri per liquidi.L'applicazione più comune per il solfato di rame era la combinazione con il bromuro di potassio per produrre candeggina al bromuro di rame per intensificare e tonificare.Alcuni fotografi hanno utilizzato il solfato di rame come vincolo negli sviluppatori di solfato ferroso utilizzati nel processo al collodio.
Il solfato di rame è un integratore nutritivo e coadiuvante tecnologico più spesso utilizzato nella forma pentaidrato.Questa forma si presenta come cristalli triclinici grandi, blu intenso o blu oltremare, come granuli blu o come polvere azzurra.L'ingrediente viene preparato mediante la reazione dell'acido solforico con l'ossido rameico o con il rame metallico.Può essere utilizzato nel latte artificiale.È anche chiamato solfato rameico.
Il solfato di rame (II) può essere impiegato per i seguenti studi:
Come catalizzatore per l'acetilazione di alcoli e fenoli in assenza di solventi.
Comporre l'elettrolita per l'elettrodeposizione dei precursori Cu-Zn-Sn, necessario per la preparazione di film sottili Cu2ZnSnS4 (CZTS).
Come catalizzatore dell'acido di Lewis per la disidratazione degli alcoli.5