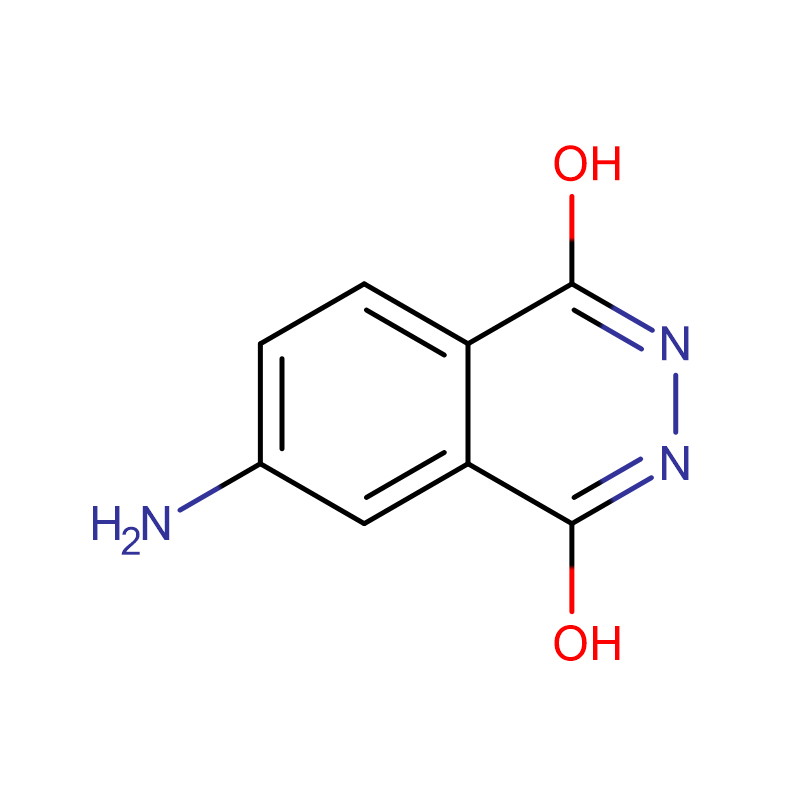
4-Aminoftalidrazide AMPPD Cas:3682-14-2 Da giallo chiaro ad ambrato a verde scuro da polvere a grumi
| Numero di catalogo | XD90156 |
| nome del prodotto | 4-amminoftalidrazide |
| CAS | 3682-14-2 |
| Formula molecolare | C8H7N3O2 |
| Peso molecolare | 177.16 |
| Dettagli di archiviazione | Conservare a RT |
Specifiche di prodotto
| Aspetto | Polvere da giallo chiaro ad ambrato a verde scuro fino a grumo |
| Assy | ≥98,0% |
| Densità | 1.433 |
| Punto di fusione | 300ºC |
| Punto di ebollizione | 633°C a 760 mmHg |
| punto d'infiammabilità | 336,7°C |
| Solubilità | Solubile in idrossido di ammonio, carbonato di sodio o altra base. |
1. Abbiamo analizzato e confrontato l'effetto di cinque antistaminici H1 sul burst ossidativo stimolato a livello extra e intracellulare di leucociti polimorfonucleati umani isolati e stimolati. Il burst ossidativo di neutrofili umani isolati è stato studiato mediante chemiluminescenza potenziata con luminolo e isoluminolo. Quanto segue L'ordine di classificazione della potenza degli antistaminici H1 per ridurre la chemiluminescenza è stato valutato a livello extracellulare: dithiaden> loratadina> clorfeniramina> bromfeniramina> feniramina e nel sito intracellulare: loratadina> dithiaden. Gli antistaminici H1 differiscono sostanzialmente in base alla loro struttura chimica nella soppressione del burst ossidativo sia a livello extra - e sito intracellulare di neutrofili umani stimolati isolati.
2. I sistemi di chemiluminescenza potenziati da isoluminol o luminol in combinazione con una perossidasi sono metodi sensibili per il rilevamento di specie reattive dell'ossigeno (ROS) generate dalla NADPH ossidasi dei fagociti.I due substrati amplificatori sono strutturalmente molto simili, differiscono solo per la posizione del gruppo amminico nell'anello aromatico delle molecole.Questa differenza rende l'isoluminolo una molecola meno lipofila e meno permeabile alle membrane biologiche.L'uso dell'isoluminolo è quindi limitato agli studi che riguardano la secrezione dei metaboliti dell'ossigeno.In questo studio mostriamo che i peptidi sintetici derivati dal dominio N-terminale della proteina annessina AI regolata dal calcio interferiscono con il rilevamento dei radicali in un sistema amplificato con isoluminolo, ma non in un sistema amplificato con luminolo.I peptidi derivati dall'annessina AI riducono l'emissione luminosa con isoluminolo eccitato da superossido e perossidasi di rafano (HRP) in cellule stimolate con formil-metionil-leucil-fenilalanina e forbolo mio ristato acetato, nonché da perossido di idrogeno e HRP.Il meccanismo preciso per l'inibizione non è noto.I risultati presentati suggeriscono fortemente che una risposta cellulare ridotta rilevata con chemiluminescenza amplificata con isoluminolo dovrebbe essere confermata con una tecnica alternativa per determinare il rilascio di anioni superossido e perossido di idrogeno.