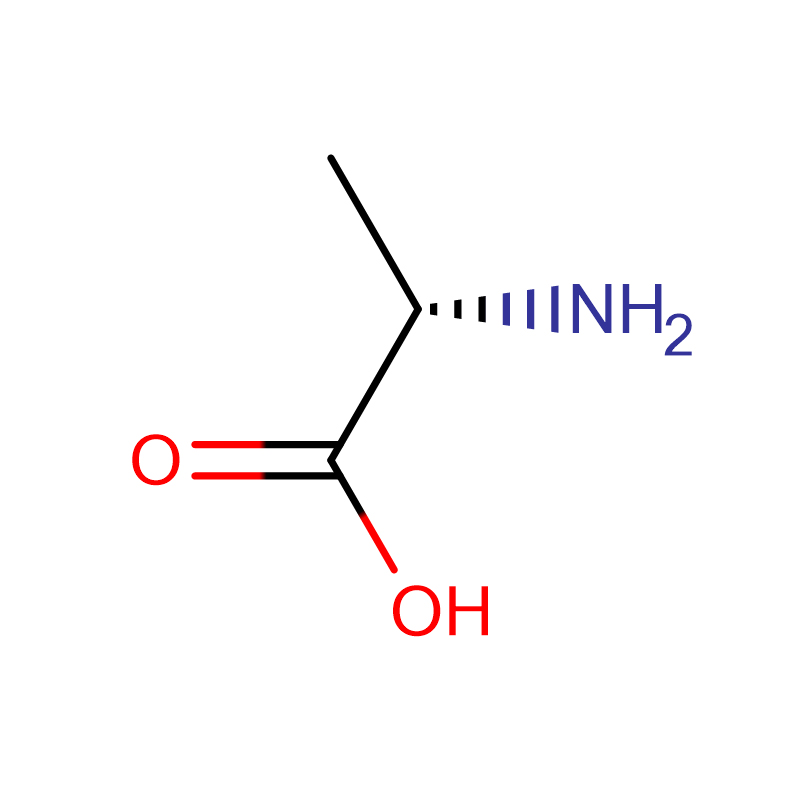
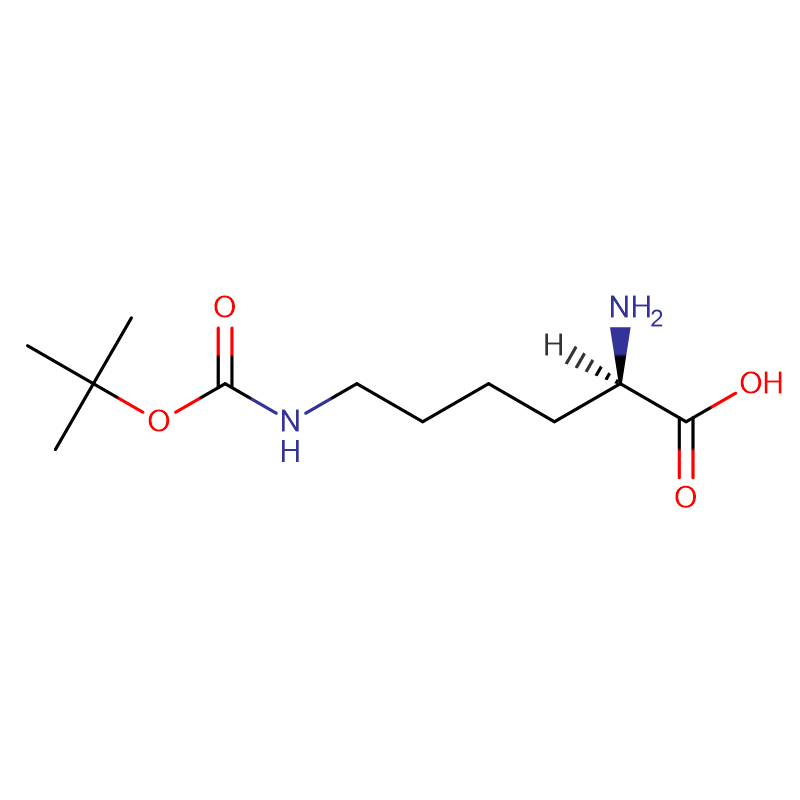
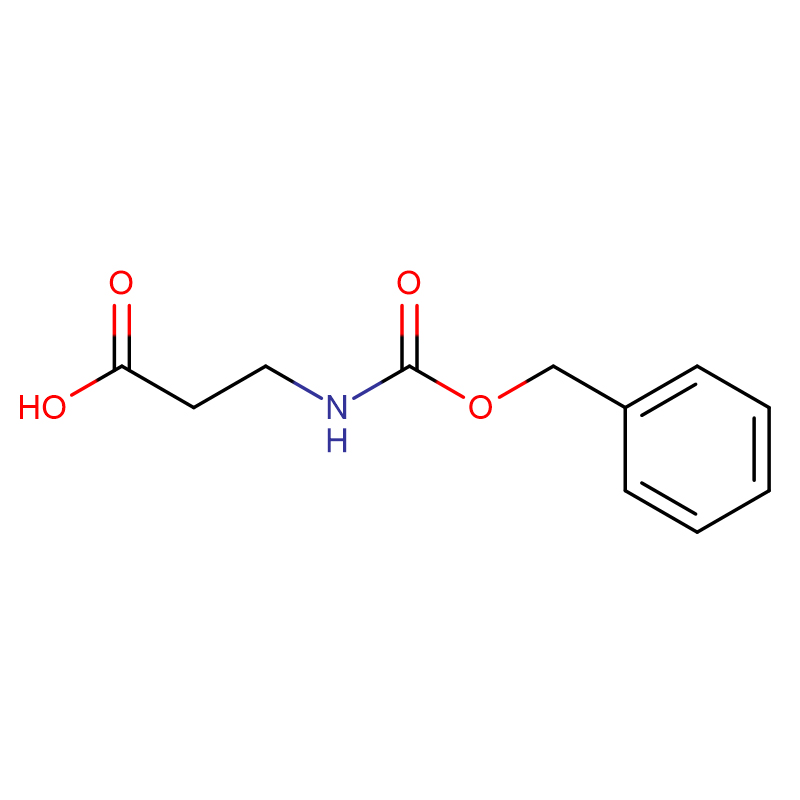
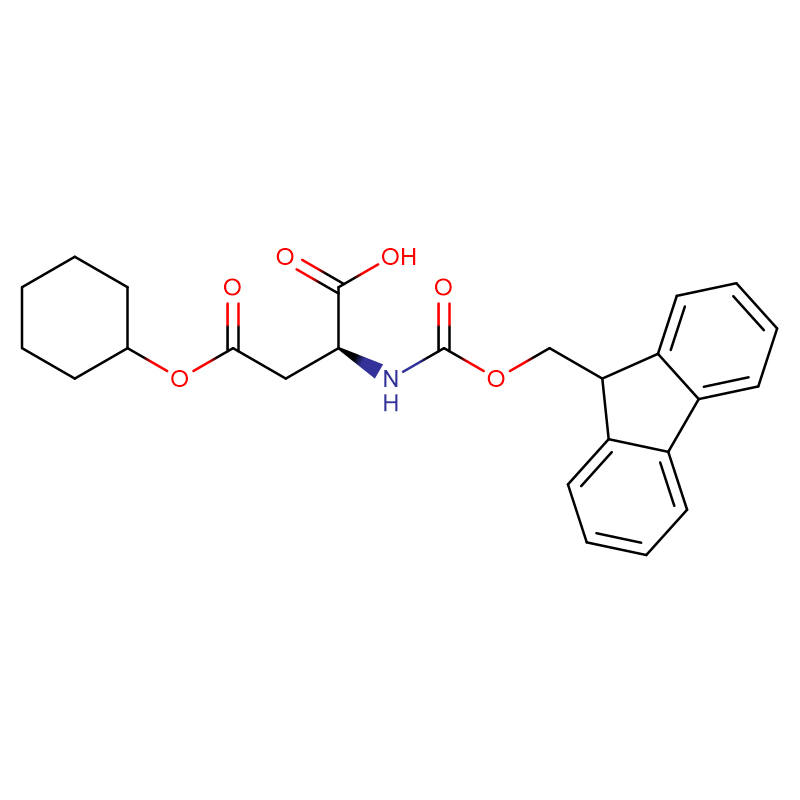
L-alanina CAS:56-41-7 99% polvere cristallina bianca
| Numero di catalogo | XD90326 |
| nome del prodotto | D-alanina |
| CAS | 338-69-2 |
| Formula molecolare | C3H7NO2 |
| Peso molecolare | 89.09 |
| Dettagli di archiviazione | Ambientale |
| Codice tariffario armonizzato | 29224985 |
Specifiche di prodotto
| Aspetto | Polvere cristallina bianca |
| Saggio | 98,5 - 101,5% |
| Rotazione specifica | da +13,7 a +15,1 |
| Metalli pesanti | <0,0015% |
| pH | 5.5 - 7 |
| SO4 | <0,03% |
| Perdita all'essiccamento | <0,2% |
| Ferro | <0,003% |
| Residuo all'accensione | <0,15% |
| Dimensione delle particelle | 200um |
| Cl | <0,05% |
| Livello di inquinanti organici persistenti | Nessun inquinante |
Le γ-glutamiltranspeptidasi (γ-GT) scindono il legame γ-glutamil ammidico del glutatione e trasferiscono il gruppo γ-glutamil rilasciato in acqua (idrolisi) o amminoacidi accettore (transpeptidazione).Questi enzimi ubiquitari svolgono un ruolo chiave nella biosintesi e degradazione del glutatione e nella disintossicazione xenobiotica.Qui riportiamo la struttura cristallina con risoluzione 3Å di Bacillus licheniformis γ-GT (BlGT) e quella del suo complesso con l-Glu.Le strutture a raggi X confermano che BlGT appartiene alla superfamiglia delle idrolasi nucleofile N-terminale e rivelano che la proteina possiede una fenditura del sito attivo aperta simile a quella riportata per l'enzima omologo da Bacillus subtilis, ma diversa da quella osservata per γ-GT umana e per γ-GT da altri microrganismi.I dati suggeriscono che il legame di l-Glu induce un riordino della coda C-terminale della subunità grande BlGT e consente l'identificazione di un cluster di residui acidi che sono potenzialmente coinvolti nel riconoscimento di uno ione metallico.Il ruolo di questi residui sulla stabilità conformazionale di BlGT è stato studiato caratterizzando l'autoprocessing, l'attività enzimatica, la denaturazione chimica e termica di quattro nuovi singoli mutanti di Ala.I risultati mostrano che la sostituzione di Asp568 con un Ala influisce sia sull'autoelaborazione che sulla stabilità strutturale della proteina.